Autor:
Monica Porter
Erstelldatum:
17 Marsch 2021
Aktualisierungsdatum:
1 Juli 2024

Inhalt
Die molare Konzentration gibt die Beziehung zwischen der Molzahl eines gelösten Stoffes und dem Volumen der Lösung an. Um die Molarität zu berechnen, können Sie mit Mol und Volumen, Masse und Volumen oder Mol und Milliliter (ml) beginnen. Wenden Sie dann mit den obigen Variablen die grundlegende Formel für die molare Konzentration an, um das richtige Ergebnis zu erhalten.
Schritte
Methode 1 von 4: Berechnen Sie die Molkonzentration aus Molzahl und Volumen
Es ist wichtig, die Grundformel zur Berechnung der Molkonzentration zu kennen. Molkonzentration gleich der Molzahl eines gelösten Stoffes geteilt durch das Volumen der Lösung in Litern. Von dort haben wir die folgende Formel: Molkonzentration = Molzahl des gelösten Stoffes / Anzahl der Liter Lösung
- Beispiel: Wie hoch ist die molare Konzentration einer Lösung, die 0,75 Mol NaCl in 4,2 Litern Lösung enthält?

Analysieren Sie das Thema. Zur Berechnung der Molkonzentration benötigen Sie die Molzahl und das Lösungsvolumen in Litern. Sie müssen diese beiden Werte aufgrund des angegebenen Themas nicht berechnen.- Beispielsweise:
- Molzahl = 0,75 Mol NaCl
- Volumen = 4,2 l
- Beispielsweise:
Teilen Sie die Anzahl der Mol durch das Volumen. Das Ergebnis der Molteilung nach Volumen ist die Anzahl der Mol pro Liter Lösung oder die molare Konzentration dieser Lösung.
- Beispiel: Molkonzentration = Molzahl des gelösten Stoffes / Anzahl der Liter Lösung = 0,75 Mol / 4,2 L = 0,17857142

Notieren Sie Ihre Ergebnisse. Runden Sie nach dem Komma auf zwei oder drei Zahlen, je nach Wunsch des Lehrers oder der Aufgabe. Wenn Sie Ihre Ergebnisse aufzeichnen, kürzen Sie "molare Konzentration" mit "M" ab und geben Sie das chemische Symbol des gelösten Stoffs an.- Beispielsweise: 0,179 M NaCl
Methode 2 von 4: Berechnung der Molkonzentration aus Masse und Volumen
Es ist notwendig, die Grundformel zur Berechnung der Molkonzentration zu kennen. Die molare Konzentration zeigt die Beziehung zwischen der Molzahl eines gelösten Stoffes und dem Volumen der Lösung. Die Formel für die molare Konzentration lautet wie folgt: Molkonzentration = Konzentration des gelösten Stoffes / Anzahl der Liter Lösung
- Problembeispiel: Berechnen Sie die Molzahl der Lösung beim Auflösen von 3,4 g KMnO4 in 5,2 Liter Wasser.

Analysieren Sie das Thema: Um die molare Konzentration zu ermitteln, benötigen Sie die Anzahl der Mol und das Volumen der Lösung in Litern. Wenn diese Werte nicht angegeben sind, Sie jedoch das Volumen und die Masse der Lösung kennen, können Sie die Anzahl der Mol gelösten Stoffs bestimmen, bevor Sie die molare Konzentration berechnen.- Beispielsweise:
- Gewicht = 3,4 g KMnO4
- Volumen = 5,2 l
- Beispielsweise:
Berechnen Sie das Massenmolekül des gelösten Stoffes. Um die Anzahl der Mol gelösten Stoffes aus dieser Masse oder Gramm gelösten Stoffs zu berechnen, müssen Sie zuerst das Massenmolekül des gelösten Stoffes bestimmen. Das Massenmolekül eines gelösten Stoffes kann durch Zugabe des Massenatoms jedes Elements in die Lösung bestimmt werden. Verwenden Sie das Periodensystem der Elemente, um das kubische Atom jedes Elements zu ermitteln.
- Beispielsweise:
- Massenatom von K = 39,1 g
- Massenatom von Mn = 54,9 g
- Massenatom von O = 16,0 g
- Gesamtatome der Masse = K + Mn + O + O + O + O = 39,1 + 54,9 + 16 + 16 + 16 + 16 = 158,0 g
- Beispielsweise:
Konvertieren Sie Gramm in Mol. Sobald Sie eine Molmasse haben, müssen Sie die Anzahl der Gramm gelösten Stoffs in der Lösung mit dem äquivalenten Umrechnungsfaktor von 1 Mol pro Molmasse des gelösten Stoffs multiplizieren. Das Ergebnis dieser Multiplikation ist die Anzahl der Mol des gelösten Stoffes.
- Beispiel: Gramm gelöster Stoff * (1 / Molmasse gelösten Stoffes) = 3,4 g * (1 Mol / 158 g) = 0,0215 Mol
Teilen Sie die Anzahl der Mol durch die Anzahl der Liter. Nachdem Sie die Anzahl der Mol berechnet haben und diese Zahl durch das Volumen der Lösung in Litern dividiert haben, erhalten Sie die molare Konzentration dieser Lösung.
- Beispiel: Molkonzentration = Molzahl des gelösten Stoffes / Anzahl der Liter Lösung = 0,0215 Mol / 5,2 L = 0,004134615
Notieren Sie Ihre Ergebnisse. Sie müssen die vom Lehrer geforderten Ergebnisse aufrunden, normalerweise zwei bis drei Zahlen nach einem Komma. Wenn Sie das Ergebnis schreiben, kürzen Sie außerdem "molare Konzentration" als "M" ab und begleiten Sie das chemische Symbol des gelösten Stoffs.
- Beispielsweise: 0,004 M KMnO4
Methode 3 von 4: Berechnen Sie die molare Konzentration aus der Anzahl der Mol und Milliliter der Lösung
Müssen die Formel für die molare Konzentration kennen. Berechnung der molaren Konzentration. Sie müssen die Molzahl des gelösten Stoffes pro Liter Lösung berechnen, nicht den Milliliter der Lösung. Die allgemeine Formel zur Berechnung der Molkonzentration lautet: molare Konzentration = Anzahl der Mol gelösten Stoffes / Anzahl der Liter Lösung
- Beispiel: Berechnen Sie die molare Konzentration einer Lösung, die 1,2 Mol CaCl enthält2 in 2905 Milliliter Wasser.
Analysieren Sie das Thema. Zur Berechnung der Molkonzentration benötigen Sie die Molzahl des gelösten Stoffes und das Volumen der Lösung in Litern. Wenn das Lösungsvolumen im Problem in Millilitern angegeben ist, rechnen Sie es vor der Berechnung in das entsprechende Volumen in Litern um.
- Beispielsweise:
- Molzahl = 1,2 Mol CaCl2
- Volumen = 2905 ml
- Beispielsweise:
Milliliter in Liter umrechnen. Teilen Sie die Anzahl der Milliliter durch 1000, um die Lösung von Millilitern in Liter umzurechnen, da jeder Liter 1000 Millilitern entspricht. Sie können Milliliter auch in Liter umrechnen, indem Sie den Dezimalpunkt um 3 Stellen nach links verschieben.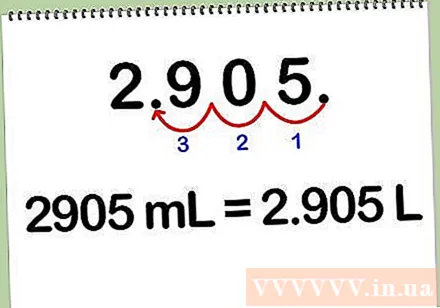
- Zum Beispiel: 2905 ml * (1 l / 1000 ml) = 2.905 l
Teilen Sie die Anzahl der Mol durch die Anzahl der Liter. Nachdem Sie die Anzahl der Liter festgelegt haben, können Sie die molare Konzentration berechnen, indem Sie die Anzahl der Mol durch die Anzahl der Liter Lösung dividieren.
- Beispiel: Molkonzentration = Molzahl des gelösten Stoffes / Anzahl der Liter Lösung = 1,2 Mol CaCl2 / 2,905 L = 0,413080895
Notieren Sie Ihre Ergebnisse. Denken Sie daran, das Ergebnis auf zwei oder drei Kommas oder auf Wunsch Ihres Lehrers zu runden. Wenn Sie das Ergebnis aufzeichnen, kürzen Sie "molare Konzentration" als "M" und dann als chemisches Symbol für den gelösten Stoff ab.
- Beispielsweise: 0,413 M CaCl2
Methode 4 von 4: Zusätzliche Übung
Berechnen Sie die molare Konzentration einer Lösung, wenn 5,2 g NaCl in 800 ml Wasser gelöst sind. Bestimmen Sie die vom Problem angegebenen Werte: Masse in Gramm und Volumen in Millilitern.
- Masse = 5,2 g NaCl
- Volumen = 800 ml Wasser
Finden Sie das Massenmolekül von NaCl, indem Sie das kubische Atom des Na-Elements und das kubische Atom von Cl hinzufügen.
- Massenatom von Na = 22,99 g
- Massenatom von Cl = 35,45 g
- Massenmoleküle von NaCl = 22,99 + 35,45 = 58,44 g
Multiplizieren Sie die Masse des gelösten Stoffes mit dem molaren Umrechnungsfaktor. In diesem Beispiel beträgt die Molekularmasse von NaCl 58,44 g, der Umrechnungsfaktor beträgt also "1 mol / 58,44 g".
- Anzahl der NaCl-Mol = 5,2 g NaCl * (1 Mol / 58,44 g) = 0,8898 Mol = 0,09 Mol
Teilen Sie 800 ml Wasser durch 1000, Sie erhalten das Wasservolumen in Litern.
- Sie können auch 800 ml mit dem Umrechnungsfaktor von 1 l / 1000 ml von Milliliter zu Liter multiplizieren.
- Um den Multiplikationsprozess wie oben zu verkürzen, können Sie den Dezimalpunkt 3 Stellen nach links verschieben.
- Volumen = 800 ml * (1 l / 1000 ml) = 800 ml / 1000 ml = 0,8 l
Teilen Sie die Molzahl des gelösten Stoffes durch das Volumen der Lösung in Litern. Um die molare Konzentration zu berechnen, müssen Sie 0,09 Mol gelösten Stoff (in diesem Fall NaCl) durch das Volumen der Lösung in Litern dividieren.
- Molkonzentration = Molzahl des gelösten Stoffes / Anzahl der Liter Lösung = 0,09 Mol / 0,8 L = 0,1125 Mol / L.
Notieren Sie das Endergebnis. Runden Sie das Ergebnis auf zwei oder drei Zahlen nach dem Komma ab und kürzen Sie "molare Konzentration" mit "M" zusammen mit dem Symbol für gelöste Chemikalien ab.
- Ergebnis: 0,11 M NaCl