Autor:
Lewis Jackson
Erstelldatum:
12 Kann 2021
Aktualisierungsdatum:
1 Juli 2024

Inhalt
Die Bestimmung der Anzahl der Neutronen in einem Atom ist recht einfach. Sie müssen nicht einmal Experimente durchführen. Um die Anzahl der Neutronen in einem normalen Atom oder Isotop zu berechnen, müssen Sie nur ein Periodensystem bereithalten und den Anweisungen folgen.
Schritte
Methode 1 von 2: Bestimmen Sie die Anzahl der Neutronen in einem normalen Atom
Bestimmen Sie die Position des Elements im Periodensystem. Als Beispiel finden wir das Element Osmium (Os) in der sechsten Reihe von oben.
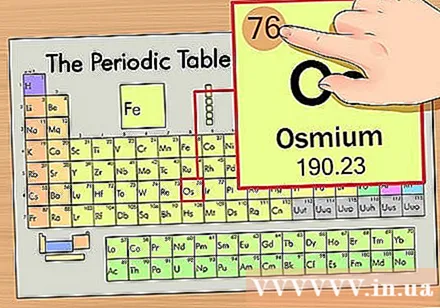
Finden Sie die Ordnungszahl des Elements. Dies ist die auffälligste Zahl, die an jedem Element vorbeigeht und über dem Hauptsymbol liegt (auf der von uns verwendeten Tafel gibt es keine anderen Zahlen). Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. Os ist die Zahl 76, was bedeutet, dass ein Osmiumatom 76 Protonen enthält.- Die Anzahl der Protonen ändert sich in einem Element nie. es ist im Wesentlichen das bestimmende Merkmal eines Elements.
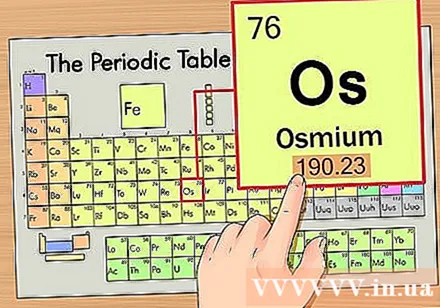
Finden Sie das Atomgewicht des Elements. Diese Zahl befindet sich normalerweise unter dem Hauptsymbol. Beachten Sie, dass das Periodensystem in diesem Beispiel nur eine Ordnungszahl und kein Atomgewicht hat. Nicht alle Periodensysteme. Osmium hat ein Atomgewicht von 190,23.
Runden Sie das Atomgewicht auf die nächste ganze Zahl, um die Atommasse zu erhalten. Zum Beispiel würde 190,23 auf 190 gerundet, so dass die Atommasse von Osmium 190 beträgt.- Das Atomgewicht ist der Durchschnitt der Isotope desselben chemischen Elements, weshalb es normalerweise keine ganze Zahl ist.
Subtrahieren Sie die Ordnungszahl von der Atommasse. Da der größte Teil der Atommasse die Masse der Protonen und Neutronen ist, subtrahieren Sie die Anzahl der Protonen von der Atommasse (d. H. Der Ordnungszahl) Anzahl Ermitteln Sie die Anzahl der Neutronen im Atom. Die Zahl nach dem Dezimalpunkt repräsentiert die sehr kleine Elektronenmasse im Atom. In diesem Beispiel haben wir: 190 (Massenatom) - 76 (Anzahl der Protonen) = 114 (Anzahl der Neutronen).
Merke dir das Rezept. Um die Anzahl der Neutronen zu ermitteln, wenden wir einfach die folgende Formel an: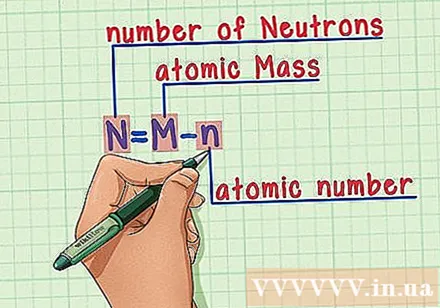
- N = M - n
- N = Anzahl der Neutronen
- M = Atommasse
- n = Ordnungszahl
- N = M - n
Methode 2 von 2: Bestimmen Sie die Anzahl der Neutronen im Isotop
Bestimmen Sie die Position des Elements im Periodensystem. Nehmen wir als Beispiel das Element Kohlenstoff-14-Isotop. Da die Isotopenform von Kohlenstoff-14 einfach Kohlenstoff (C) ist, suchen Sie im Periodensystem (zweite Reihe von oben) nach Kohlenstoff.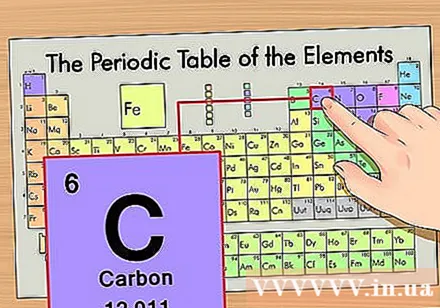
Finden Sie die Ordnungszahl des Elements. Dies ist die auffälligste Zahl, die an jedem Element vorbeigeht und über dem Hauptsymbol liegt (auf der von uns verwendeten Tafel gibt es keine anderen Zahlen). Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. C ist Nummer 6, was bedeutet, dass ein Kohlenstoffatom 6 Protonen enthält.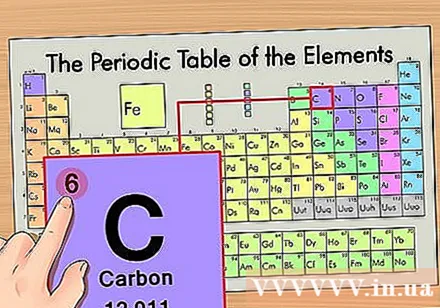
Finde Atommasse. Dies ist bei Isotopen sehr einfach, da sie nach der Atommasse benannt sind. Zum Beispiel hätte Kohlenstoff-14 eine Atommasse von 14. Sobald Sie die Atommasse des Isotops gefunden haben, sind die verbleibenden Schritte zum Ermitteln der Anzahl der Neutronen dieselben wie die eines normalen Atoms.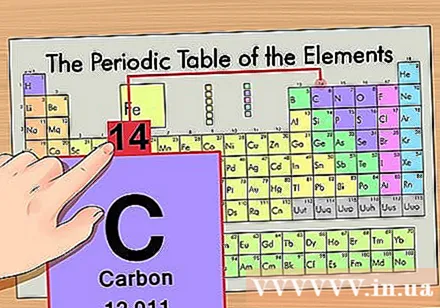
Subtrahieren Sie die Ordnungszahl von der Atommasse. Da der größte Teil der Atommasse die Masse der Protonen und Neutronen ist, subtrahieren Sie die Anzahl der Protonen von der Atommasse (d. H. Der Ordnungszahl) Anzahl Ermitteln Sie die Anzahl der Neutronen im Atom. Die Zahl nach dem Dezimalpunkt repräsentiert die sehr kleine Elektronenmasse im Atom. In diesem Beispiel haben wir: 14 (Massenatom) - 6 (Anzahl der Protonen) = 8 (Anzahl der Neutronen).
Merke dir das Rezept. Um die Anzahl der Neutronen zu ermitteln, wenden wir die folgende Formel an: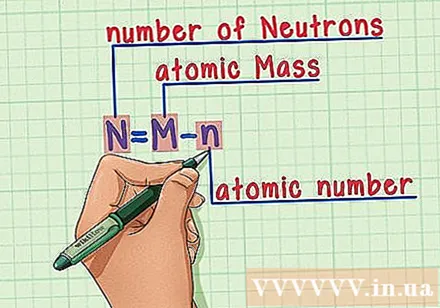
- N = M - n
- N = Anzahl der Neutronen
- M = Atommasse
- n = Ordnungszahl
- N = M - n
Rat
- Die Masse eines Elements ist größtenteils die Masse von Protonen und Neutronen, während die Massen von Elektronen und anderen Elementen vernachlässigbar sind (fast Null). Da die Masse des Protons ungefähr gleich der Masse des Neutrons ist und die Ordnungszahl die Anzahl der Protonen darstellt, müssen wir nur die Anzahl der Protonen von der Gesamtmasse subtrahieren.
- Wenn Sie sich nicht an die Bedeutung der Zahlen im Periodensystem erinnern, denken Sie daran, dass das Periodensystem normalerweise auf Ordnungszahlen (d. H. Der Anzahl der Protonen) basiert, beginnend bei 1 (Wasserstoff) und inkrementierend ein Wort von links nach rechts, endend mit 118 (Ununoctium). Da die Anzahl der Protonen ein identifizierendes Merkmal jedes Atoms ist, ist es die einfachste Eigenschaft, auf der die Elemente angeordnet sind. (Zum Beispiel ist ein Atom mit 2 Protonen immer Helium, genauso wie ein Atom mit 79 Protonen immer Gold ist.)
Quellen und Zitate
- Interaktives Periodensystem



