Autor:
Bobbie Johnson
Erstelldatum:
10 April 2021
Aktualisierungsdatum:
1 Juli 2024

Inhalt
- Schritte
- Teil 1 von 2: Bereiten Sie die Ausrüstung vor
- Teil 2 von 2: Führe ein Experiment durch
- Tipps
- Warnungen
- Was brauchst du
Wasserspaltungsverfahren (H2O) in seine Bestandteile (Wasserstoff und Sauerstoff) unter Verwendung von Strom wird als Elektrolyse bezeichnet. Die bei der Elektrolyse anfallenden Gase können allein genutzt werden – beispielsweise dient Wasserstoff als einer der saubersten Energieträger. Auch wenn der Name dieses Prozesses ein wenig clever klingen mag, ist es tatsächlich einfacher, als es den Anschein hat, wenn Sie über die richtige Ausrüstung, das richtige Wissen und ein wenig Erfahrung verfügen.
Schritte
Teil 1 von 2: Bereiten Sie die Ausrüstung vor
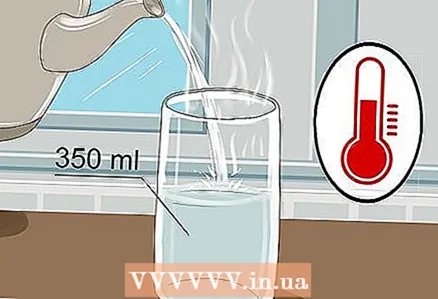 1 Nehmen Sie ein 350 ml Glas und gießen Sie warmes Wasser hinein. Das Glas muss nicht randvoll gefüllt werden, es genügt ein wenig Wasser. Kaltes Wasser reicht aus, obwohl warmes Wasser den Strom besser leitet.
1 Nehmen Sie ein 350 ml Glas und gießen Sie warmes Wasser hinein. Das Glas muss nicht randvoll gefüllt werden, es genügt ein wenig Wasser. Kaltes Wasser reicht aus, obwohl warmes Wasser den Strom besser leitet. - Sowohl Leitungswasser als auch Mineralwasser reichen aus.
- Warmes Wasser hat eine geringere Viskosität, wodurch sich Ionen leichter bewegen können.
 2 1 Esslöffel (20 Gramm) Kochsalz in Wasser auflösen. Gießen Sie Salz in ein Glas und rühren Sie das Wasser um, damit es sich auflöst. Dadurch entsteht eine Kochsalzlösung.
2 1 Esslöffel (20 Gramm) Kochsalz in Wasser auflösen. Gießen Sie Salz in ein Glas und rühren Sie das Wasser um, damit es sich auflöst. Dadurch entsteht eine Kochsalzlösung. - Natriumchlorid (also Kochsalz) ist ein Elektrolyt, der die elektrische Leitfähigkeit von Wasser erhöht. Wasser allein leitet den Strom nicht gut.
- Nachdem Sie die elektrische Leitfähigkeit des Wassers erhöht haben, fließt der von der Batterie erzeugte Strom leichter durch die Lösung und spaltet die Moleküle effektiver in Wasserstoff und Sauerstoff auf.
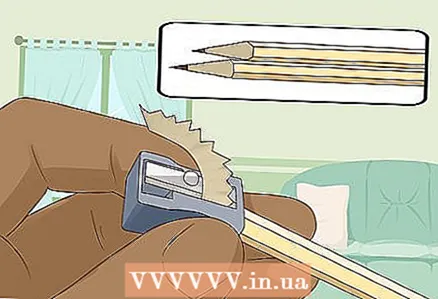 3 Spitze zwei harte-weiche Bleistifte an beiden Enden, um die Mine freizulegen. Vergessen Sie nicht, den Radiergummi von Ihren Bleistiften zu entfernen. An beiden Enden sollte ein Graphitstab herausragen.
3 Spitze zwei harte-weiche Bleistifte an beiden Enden, um die Mine freizulegen. Vergessen Sie nicht, den Radiergummi von Ihren Bleistiften zu entfernen. An beiden Enden sollte ein Graphitstab herausragen. - Die Graphitstäbe dienen als isolierte Elektroden, an die Sie die Batterie anschließen.
- Graphit ist für dieses Experiment gut geeignet, da es sich in Wasser nicht auflöst oder korrodiert.
 4 Schneide einen Karton aus, der groß genug ist, um auf dem Glas zu liegen. Verwenden Sie ein ziemlich dickes Stück Pappe, das nicht durchhängt, nachdem Sie zwei Löcher darin gestanzt haben. Schneiden Sie ein quadratisches Stück aus einem Schuhkarton oder ähnlichem.
4 Schneide einen Karton aus, der groß genug ist, um auf dem Glas zu liegen. Verwenden Sie ein ziemlich dickes Stück Pappe, das nicht durchhängt, nachdem Sie zwei Löcher darin gestanzt haben. Schneiden Sie ein quadratisches Stück aus einem Schuhkarton oder ähnlichem. - Der Karton wird verwendet, um die Bleistifte im Wasser zu halten, damit sie die Seiten und den Boden des Glases nicht berühren.
- Karton ist nicht leitend, sodass Sie ihn sicher auf ein Glas legen können.
 5 Verwenden Sie Bleistifte, um zwei Löcher in den Karton zu stechen. Durchstechen Sie den Karton mit Bleistiften - in diesem Fall werden sie fest geklemmt und rutschen nicht. Achten Sie darauf, dass der Graphit nicht die Seiten oder den Boden des Glases berührt, da er sonst das Experiment stört.
5 Verwenden Sie Bleistifte, um zwei Löcher in den Karton zu stechen. Durchstechen Sie den Karton mit Bleistiften - in diesem Fall werden sie fest geklemmt und rutschen nicht. Achten Sie darauf, dass der Graphit nicht die Seiten oder den Boden des Glases berührt, da er sonst das Experiment stört.
Teil 2 von 2: Führe ein Experiment durch
 1 Schließen Sie einen Draht mit Krokodilklemmen an jeden Batteriepol an. Die Batterie dient als Stromquelle, und durch die Drähte mit Klemmen und Graphitstäben gelangt der Strom ins Wasser.Verbinden Sie einen Draht mit einer Klemme mit dem Pluspol und den anderen mit dem Minuspol der Batterie.
1 Schließen Sie einen Draht mit Krokodilklemmen an jeden Batteriepol an. Die Batterie dient als Stromquelle, und durch die Drähte mit Klemmen und Graphitstäben gelangt der Strom ins Wasser.Verbinden Sie einen Draht mit einer Klemme mit dem Pluspol und den anderen mit dem Minuspol der Batterie. - Verwenden Sie eine 6-Volt-Batterie. Wenn Sie keine haben, können Sie stattdessen eine 9-Volt-Batterie verwenden.
- Eine geeignete Batterie erhalten Sie im Elektrofachhandel oder im Supermarkt.
 2 Verbinden Sie die anderen Enden der Drähte mit den Stiften. Befestigen Sie die Metalldrahtklemmen fest an den Graphitstäben. Möglicherweise müssen Sie noch etwas Holz von den Bleistiften abziehen, damit die Clips nicht von den Graphitstäben rutschen.
2 Verbinden Sie die anderen Enden der Drähte mit den Stiften. Befestigen Sie die Metalldrahtklemmen fest an den Graphitstäben. Möglicherweise müssen Sie noch etwas Holz von den Bleistiften abziehen, damit die Clips nicht von den Graphitstäben rutschen. - Dadurch schließen Sie den Stromkreis und Strom von der Batterie fließt durch das Wasser.
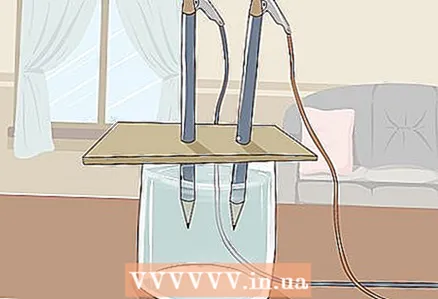 3 Legen Sie den Karton so auf das Glas, dass die freien Enden der Stifte in das Wasser eingetaucht sind. Der Karton sollte groß genug sein, um auf dem Glas zu liegen. Achten Sie darauf, die korrekte Platzierung der Stifte nicht zu stören.
3 Legen Sie den Karton so auf das Glas, dass die freien Enden der Stifte in das Wasser eingetaucht sind. Der Karton sollte groß genug sein, um auf dem Glas zu liegen. Achten Sie darauf, die korrekte Platzierung der Stifte nicht zu stören. - Damit das Experiment gelingt, darf der Graphit die Wände und den Boden des Glases nicht berühren. Überprüfen Sie dies noch einmal und passen Sie die Stifte gegebenenfalls an.
 4 Beobachten Sie, wie sich das Wasser in Wasserstoff und Sauerstoff aufspaltet. Aus den im Wasser eingetauchten Graphitstäben steigen Gasblasen auf. Dies sind Wasserstoff und Sauerstoff. Am Minuspol wird Wasserstoff und am Pluspol Sauerstoff freigesetzt.
4 Beobachten Sie, wie sich das Wasser in Wasserstoff und Sauerstoff aufspaltet. Aus den im Wasser eingetauchten Graphitstäben steigen Gasblasen auf. Dies sind Wasserstoff und Sauerstoff. Am Minuspol wird Wasserstoff und am Pluspol Sauerstoff freigesetzt. - Sobald Sie die Drähte mit der Batterie und den Graphitstäben verbinden, fließt ein elektrischer Strom durch das Wasser.
- An dem Bleistift, der mit dem Minuspol verbunden ist, bilden sich weitere Gasblasen, da jedes Wassermolekül aus zwei Wasserstoffatomen und einem Sauerstoffatom besteht.
Tipps
- Wenn Sie keine Bleistifte mit Graphitschaft haben, können Sie stattdessen zwei kleine Drähte verwenden. Wickeln Sie einfach ein Ende jedes Drahtes um den entsprechenden Batteriepol und tauchen Sie das andere ins Wasser. Das Ergebnis ist das gleiche wie bei Bleistiften.
- Versuchen Sie es mit einem anderen Akku. Die Menge des fließenden Stroms hängt von der Spannung der Batterie ab, die wiederum die Spaltungsrate der Wassermoleküle beeinflusst.
Warnungen
- Wenn Sie dem Wasser einen Elektrolyten wie Salz hinzufügen, denken Sie daran, dass das Experiment eine kleine Menge eines Nebenprodukts wie Chlor erzeugt. In so kleinen Mengen ist es sicher, aber Sie können einen leichten Chlorgeruch riechen.
- Führen Sie dieses Experiment unter Aufsicht von Erwachsenen durch. Es ist mit Elektrizität und Gasen verbunden und kann daher gefährlich, wenn auch unwahrscheinlich, sein.
Was brauchst du
- Zwei hart-weiche Bleistifte
- Eine 6- oder 9-Volt-Batterie
- Glas mit einem Volumen von 350 Milliliter
- 2 Drähte mit Krokodilklemmen
- Spitzer für Bleistift
- Salz



